Сравнительный анализ бета-интерферонов,
используемых для лечения рассеянного склероза
Е.И.Гусев, Т.Л.Демина, Н.В.Хачанова
Российский государственный медицинский университет, Москва
В последние годы появилась реальная возможность лечения
рассеянного склероза (PC). Проведенные международные клинические испытания эффективности
бета-интерферона (ИНФ-b) при PC показали снижение частоты и тяжести обострений
заболевания, увеличение времени до наступления следующего обострения, а также
уменьшение активности болезни по данным МРТ. Однако прямых сравнительных плацебо-контролируемых
испытаний всех трех интерферонов-бета до настоящего времени не проводилось.
Поэтому возможно только косвенное сравнение эффективности различных препаратов
ИНФ-b при разных типах течения PC. Результаты недавно проведенных двух прямых
открытых сравнительных исследований свидетельствуют о превосходстве терапии
ИНФ-b в высокой дозе и с высокой частотой введения для достижения максимального
лечебного эффекта.
There have been considerable advances made recently
in the treatment of multile sclerosis (MS). The International clinical trials
of interferon-beta (IFN-b) in MS demonstrated the efficacy of IFN-b in reducing
the frequency and severity of relapses, increasing time to first relapse after
starting the therapy and in decreasing disease activity on MRI scans. However,
head-to-head comparative double-blind, placebo controlled trials of all three
preparations of IFN-b have not been made yet. Thus, only indirect comparative
analysis of efficacy different preparations of IFN-b in different courses of
MS is available. The data of recently reported two head-to-head comparative
single-blind trials demostrated the superior efficacy of high dose/high frequency
regimen of inter-feron beta treatment to achieve maximum therapuetic effect.
В настоящее время
после многих лет интенсивных исследований новым подходом к селективной иммунокоррекции
при рассеянном склерозе (PC) является направленное воздействие на избыточную
продукцию активирующих цитокинов и стимуляцию выработки in vivo противовоспалительных
цитокинов. К препаратам, основным действием которых является влияние на продукцию
цитокинов, относятся препараты бета-интерферона (b-ИФН), доказавшие клиническую
эффективность в ходе многоцентровых клинических испытаний двойным слепым методом.
Интерес к интерферонам в лечении PC
впервые появился в 1970-х годах и основывался на двух до сих пор не доказанных
положениях: во-первых, PC вызывается персистирующей вирусной инфекцией, на которую
можно воздействовать интерферонами, и, во-вторых, продукция интерферонов снижена
у больных PC. Точный механизм действия интерферонов при PC неизвестен. Однако
в последние годы удалось больше узнать о взаимодействии b-ИФН с интерфероновым
рецептором. Так стало понятным, что взаимодействие альфа-интерферона и бета-интерферона
происходит с разными эпитопами одного и того же рецептора, приводя к лиганд-зависимым
структурным изменениям молекулы этого рецептора и различным биологическим эффектам
[25]. Интерфероны обладают противовоспалительным, антипролиферативным и иммуномодулирующими
эффектами, и наиболее важными из них для PC являются иммуномодулирующая и противовирусная
активность. В настоящее время считается, что интерферон-бета снижает продукцию
провоспалительных цитокинов - ФНО-а и гамма-интерферона, замедляет пролиферацию
Т-клеток, стимулирует выработку противовоспалительных цитокинов - IL-10 и трансформирующего
фактора роста бета-1, снижает экспрессию молекул гисто-совместимости II класса
и молекул адгезии, тем самым уменьшая антиген-представление в ЦНС и проницаемость
гемато-энцефалического барьера [25].
Примерно у 85 % больных PC в начале
заболевания диагностируется ремитирующий тип течения (РРС). Уже через 10 лет
болезни половина пациентов с ремиттирующим течением переходит в стадию вторичного
прогрессирования (ВПРС), а через 25 лет у 90% больных с первоначальным РРС наблюдается
неуклонное прогрессирование заболевания. На разных стадиях и при разных типах
течения заболевания эффективность лечения b-ИФН может варьировать [1].
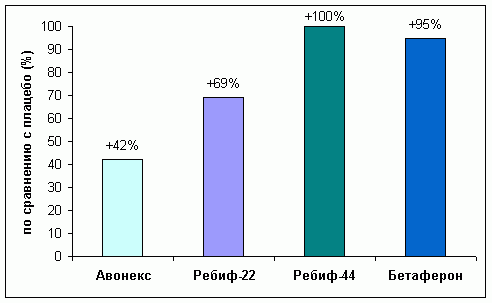
Диаграмма 1. Увеличение количества
больных без обострений (относительно плацебо).
Непрямое сравнение по данным III-ей фазы (*IFNB 1993,
**PRISMS Study Group 1998, *** Jacobs et al. 1996) при ремиттирующем течении
PC после 2 лет терапии
 |
Существует 2 типа бета-интерферона,
используемых для лечения PC - это бета-интерферон-1б (препарат Бетаферон) и
бета-интерферон-1а (препараты Ребиф и Авонекс). Бетаферон вводится через день
подкожно в дозе 8 ММЕ (250 мкг), Авонекс 1 раз в неделю внутримышечно в дозе
6 ММЕ (30 мкг), а Ребиф рекомендован 3 раза в неделю подкожно в двух лечебных
дозах - 6 ММЕ (22 мкг) и 12 ММЕ (44 мкг) [9,11,14]. Все препараты получены методом
ре-комбинантного синтеза на основе ДНК человека. Интерфероны-бета-1a нарабатываются
в культуре клеток яичника китайского хомячка, а интерферон-бета-1б - в культуре
бактериальных клеток (Е. Coli). Учитывая отсутствие согласованности в методах
определения биологической активности интерферонов, прямое сравнение активности
различных препаратов затруднено [3]. К примеру, фармакокинетические исследования
одинаковых доз Авонекса и Ребифа у здоровых лиц, вводимых внутримышечно и подкожно
соответственно, показали противоречивые результаты, что возможно объясняется
использованием различных методов для определения активности двух препаратов
в разных исследованиях, а также тем фактом, что Ph готового раствора Авонекса
составляет 7.2, а Ребифа 3.8 [3]. Проведенные фармако-динамические исследования
влияния различных доз интерферона бета-1б и интерферона бета-1а после однократного
введения на продукцию маркеров биологического ответа у здоровых лиц показали,
что доза 6 ММЕ интерферона бета-1a (Авонекс), вводимого внутримышечно примерно
эквивалентна дозе в 8 ММЕ интерферона бета-16, вводимого подкожно [24]. Рандомизированное
сравнительное исследование фармакологических и фармакодинамических эффектов
Бетаферона, вводимого в дозе 8 ММЕ подкожно через день в неделю, и Авонекса,
введенного 1 раз внутримышечно в течение недели, здоровым лицам, показало стойкое
достоверно более выраженное повышение уровня IL-10, а также неоптерина и b2-микроглобулина
на фоне терапии Бетафероном по сравнению с Авонексом (р=0.031) [22].
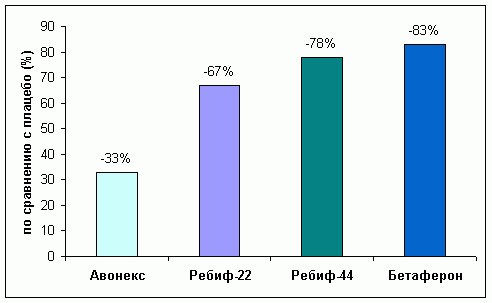
Диаграмма 2. Уменьшение
количества активных очагов по данным МРТ.
Непрямое сравнение по данным III-ей фазы (*IFNB 1993,
**PRISMS Study Group 1998, ***Jacobs et al.1996) при ремиттирующем течении
PC после 2 лет терапии
|
 |
Учитывая, что прямого сравнительного
плацебо-контролируемого исследования эффективности различных бета-интерферонов
у больных с РРС и ВПРС двойным слепым методом до настоящего времени не проводилось,
нам представляется интересным обзор и анализ литературных данных отдельных базисных
исследований, а также двух прямых сравнительных открытых исследований эффективности
b-ИФНов в лечении PC. Основными критериями активности заболевания в каждом базисном
исследовании были приняты: частота обострений в год , время от начала терапии
до наступления первого обострения, количество пациентов без обострений. Признаками
активности при МРТ-исследовании считалось появление новых очагов, возобновление
и увеличение в размерах старых очагов или усиление очагов с помощью контраста
(гадолиния). Также оценивалось: количество пациентов с подтвержденным прогрессированием
заболевания к концу исследования (увеличение показателя EDSS на 1 балл) и время
наступления подтвержденного прогрессирования.
Диаграмма 3. Уменьшение
объема поражения мозга по Т2-изображениям.
Непрямое сравнение по данным III-ей фазы (*IFNB 1993,
**PRISMS Study Group 1998, ***Jacobs et al. 1996) при ремиттирующем течении
PC после 2 лет терапии |
|
Первые исследования эффективности
бета-интерферонов при ремиттирующем PC были проведены с интерфероном бета-1б
(Бетаферон). Он отличается от природного тем, что негликолизирован, а в позиции
17 имеет вместо цистеинового амино-кислотного остатка сериновый и отсутствием
N-концевого метионинового остатка. В ходе проведения исследования, в котором
приняли участие 372 пациента с ремиттирующим PC (с EDSS от 0 до 5,5 баллов),
получавших интерферон бета-1б в дозе 1,6 ММЕ, 8 ММЕ или плацебо подкожно через
день в течение 2-х лет, было выявлено достоверное снижение частоты обострений
на 34% (р<0.009) на фоне лечения в высокой дозе (8 ММЕ) по сравнению с плацебо.
Время до наступления первого обострения от начала исследования на фоне лечения
высокой дозой Бетаферона увеличилось на 86% по сравнению с группой плацебо.
Количество пациентов, у которых не наблюдалось ни одного обострения в течение
2-х лет наблюдения в группе больных, получавших лечение ИНФb-1б в высокой дозе,
было значительно выше по сравнению с плацебо (31% против 16%, р=0.007) (диаграмма
№1). Клиническая эффективность Бетаферона была подтверждена данными МРТ, которые
показали уменьшение образования новых очагов после 2-х лет терапии на 83% (р<0.009)
(диаграмма №2) [9,10,15], при этом активность на томмограммах снижалась уже
в течение первого месяца применения Бетаферона в среднем на 75% [1]. Средний
объем пораженного белого вещества, видимый на Т2-изображениях (объем очагового
поражения мозга), увеличился на 16.5% по сравнению с исходными данными в группе
плацебо, в то время как, в группе больных, получавших ИНФb-1б , этот показатель
уменьшился на 0.8% (р=0.001) (диаграмма №3). Лечение интерфероном бета-16 в
высокой дозе также привело к уменьшению количества пациентов с подтвержденным
прогрессированием на 29%, хотя статистической значимости достигнуто не было
(р=0.16). По окончании 2-х лет терапии большинство пациентов продолжило участие
в плацебо-контролируемом исследовании. Наблюдение за этими больными с РРС в
течение 5-ти лет показало стойкий дозо-зависимый эффект [10]. Проведенный позднее
дополнительный анализ показал, что Бетаферон высоко эффективен при раннем начале
лечения, у пациентов с активным течением заболевания и не большой степенью инвалидизации
[8].
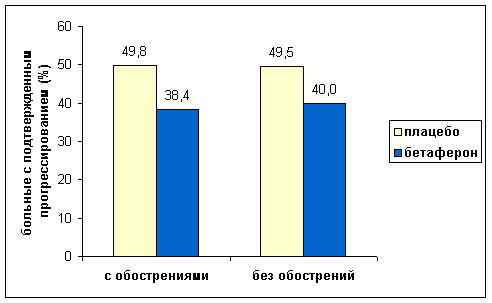
Диаграмма 4. Распределение больных
в зависимости от наличия или отсутствия обострений до начала исследования.
(* European IFNB Study in Secondary Progressive MS 1998
) при вторично-прогрессирующем течении PC после 3 лет терапии
 |
Исследование клинической эффективности
интерферона бета-1б при вторично-прогрессирующем PC проводилось в течение 3-х
лет в 32 клиниках Европы в течение 3-х лет на 718 пациентах с неврологическим
дефицитом по шкале EDSS от 3 0 до 6.5 баллов. Это было самым крупномасштабным
исследованием при PC по количеству участвовавших в нем больных. Основными критериями
эффективности в данном исследовании были количество пациентов с подтвержденным
прогрессированием и время наступления подтвержденного прогрессирования. Сопоставление
результатов лечения Бетафероном с группой плацебо показало, что количество пациентов
с подтвержденным прогрессированием было на 24.4% меньше в лечебной группе, чем
в группе плацебо (р=0.0056) [6]. Интересным оказался тот факт, что после разделения
больных на подгруппы: тех, у кого наблюдались обострения за последние 2 года
до начала исследования и тех, у кого сохранялось стойкое прогрессирование болезни,
эффективность терапии Бетафероном в обеих подгруппах была одинаковой (диаграмма
№4). После разделения больных на подгруппы по принципу наличия или отсутствия
обострений в течение всего исследования эффективности терапии была также одинаковой,
т.е. не зависела от обострений (диаграмма №5). Анализ эффективности терапии
в зависимости от степени инвалидизации по шкале EDSS показал, что приостановление
дальнейшего развития болезни независимым от исходной степени инвалидизации [8].
Оценка вероятности задержки прогрессирования болезни показала, что эффект проявлялся
спустя 9 месяцев терапии и становился достоверным уже через 12 месяцев [6].
Данное исследование подтвердило, что эффекты бета-интерферона-1б на активность
заболевания при вторично-прогрессирующем PC соответствует эффектам в отношении
снижения частоты и выраженности обострений при ремиттирующем течении заболевания
[6]. МРТ-исследование, проводимое в рамках многоцентрового плацебо-контролируемого
испытания эффективности Бетаферона у больных с вторично-прогрессирующим течением
PC, показало позитивный эффект Бетаферона на выраженность локальной атрофии,
т.е. количество и объем очагов гипоинтенсивности на Т1-изображениях (так называемых
«черных дыр»), которые лучше коррелируют со степенью инвалидизации по шкале
EDSS, чем Т2-изображения [1]. При сравнении данных 85 пациентов с вторично-прогрессирующим
PC, получавших Бетаферон или плацебо, у которых до лечения в среднем был одинаковый
объем Т1-очагов, через 3 года в группе плацебо объем очагов увеличился на 41,8
% по сравнению с исходным (р=0.0002), а при лечении Бетафероном на 23,2 % (р=0.006).
Таким образом, терапия Бетафероном позволила достоверно уменьшить образование
«черных дыр», т.е. выраженность локальной атрофии на 45 % по сравнению с группой
плацебо (р=0.0003) [4]. Сравнительное исследование частоты неблагоприятного
перехода от ремиттирующего течения PC к вторично-прогрессирующему типу течения
у больных PC, получавших длительный курс лечения бета интерфероном, по сравнению
с естественным течением заболевания показало, что после курса лечения бета интерфероном
вероятность неблагоприятной смены типа течения PC достоверно уменьшается при
любой длительности заболевания (р=0.03) [2].
Диаграмма 5. Распределение больных
в зависимости от наличия или отсутствия обострений во время исследования.
(* European IFNB Study in Secondary Progressive MS 1998)
при вторично-прогрессирующем течении PC после 3 лет терапии
 |
Интерферон бета-1а является также
биотехнологическим продуктом, по структуре он аналогичен естественному белку.
Испытания клинической эффективности интерферона бета-1a (Ребиф) при ремиттирующем
течение PC проводились в 22 клиниках мира (исследование PRISMS). В этом исследовании
участие приняли 560 пациентов с неврологическим дефицитом по шкале EDSS от 0
до 5.0. Пациенты были рандомизированы на 3 группы, получавших 22 мкг (6 ММЕ)
интерферона бета-1a 3 раза в неделю подкожно, 44 мкг (12 ММЕ) интерферона бета-1a
3 раза в неделю подкожно, либо плацебо. Результаты данного исследования после
2-х лет наблюдения показали, что по сравнению с группой плацебо лечение в дозе
22 мкг снизило частоту обострений в год на 29%, а в дозе 44 мкг на 32% (р<0.005).
Время до наступления первого обострения от начала исследования на фоне лечения
высокой дозой Ребифа увеличилось на 113% , а в дозе 22 мкг на 70% по сравнению
с группой плацебо. Количество пациентов, у которых не наблюдалось ни одного
обострения в течение 2-х лет наблюдения в группе больных, получавших лечение
ИНФb-1а в высокой дозе, достоверно увеличилось вдвое (р<0.005 ) и на 69%
в группе больных, получавших Ребиф 22 мкг, по сравнению с плацебо (диаграмма
№1) [12,16]. Оценка тяжести заболевания по данным МРТ показала уменьшение количества
активных очагов на 78% на фоне лечения Ребифом в высокой дозе и на 67% в дозе
22 мкг по сравнению с плацебо (р<0.0001) (диаграмма №2). Объем очагового
поражения мозга, оцениваемый по Т2-изображениям, уменьшился на 3.8% на фоне
терапии ИНФb-1а в высокой дозе , в то время как, в группе плацебо этот показатель
увеличился на 10.9%. по сравнению с исходным. Таким образом, объем очагового
поражения мозга на фоне терапии уменьшилась на 14.7% (р<0.0001) (диаграмма
№3). Недавно опубликованы данные о положительном влиянии интерферона бета-la
у больных с ремиттирующим течением PC на объем очагов на Т1-изображениях, являющихся
косвенным маркером выраженности локальной атрофии мозга [20].
По окончании 2-х лет испытаний исследование
было продолжено еще в течение двух лет, при этом пациенты, получавшие плацебо,
были рерандомизированы на группы, получавших либо Ребиф 22 мкг х 3 раза в неделю
подкожно, либо Ребиф 44 мкг х 3 раза в неделю подкожно. Анализ длительного наблюдения
(в течение 4-х лет) показал снижение частоты обострений на 50% у рерандомизированных
больных, получавших ранее плацебо, а также преимущества терапии в высокой дозе
[18].
Помимо влияния на среднегодовую частоту обострений, терапия Бетафероном и Ребифом
позволила достоверно снизить частоту средних и тяжелых обострений (диаграмма
№6), число госпитализаций, необходимость проведения курсов кортикостероидной
терапии [10,16].
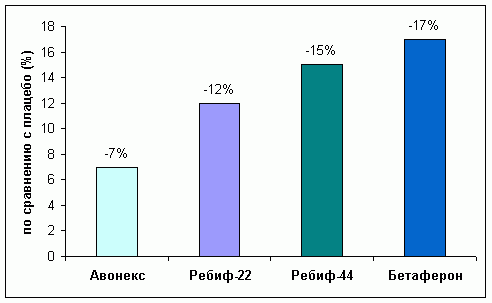
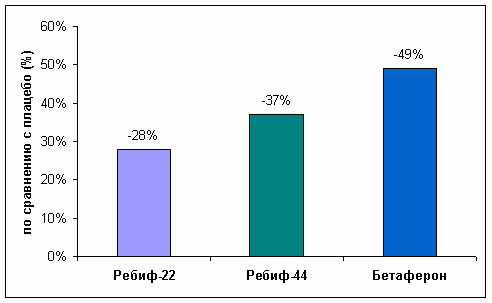
Диаграмма 6. Уменьшение частоты средних
и тяжелых обострений (относительно плацебо).
Непрямое сравнение по данным III-ей фазы (*IFNB 1993, **PRISMS Study Group
1998) при ремиттирующем течении PC после 2 лет терапии
 |
В 2001 году опубликованы результаты испытаний ИНФb-1а (Ребиф) при вторично-прогрессирующем
PC (SPECTRIMS). В этом исследовании приняли участие 618 пациентов, рандомизированные
на 3 группы по аналогии с протоколом испытаний ребифа при РРС. Учитывая, что
основным критерием эффективности данной терапии при ВПРС является время наступления
подтвержденного прогрессирования, статистически значимого положительного эффекта
препарата на этот показатель достигнуто не было [13]. Однако, было показано
снижение частоты обострений и увеличение количества пациентов без обострений
[21]. Повторный анализ в подгруппах пациентов с обострениями до начала исследования
и без обострений показал эффективность препарата в дозе 44 мкг только у пациентов
с активным течением болезни, т.е. с сохраняющимися обострениями заболевания
[21]. Положительные клинические данные были подтверждены данными МРТ в виде
достоверного снижения количества активных очагов и уменьшения общего объема
очагового поражения головного мозга [6,21].
Многоцентровые испытания интерферона бета-la, вводимого внутримышечно в дозе
6 ММЕ 1 раз в неделю (Авонекс), включали 301 пациента с РРС. В этом исследовании
пациенты были рандомизированы на две группы: группа больных, получавших 30 мкг
(6 ММЕ) интерферона бета-la внутримышечно 1 раз в неделю или группа-плацебо.
После 2-х лет терапии Авонексом наблюдалось снижение частоты обострений в год
на 18% (р=0.04), увеличение количества пациентов без обострений на 42% (диаграмма
№1), увеличение времени до наступления первого обострения на 31% (47,3 недели
против 36,1 недели, р=0.34) [11]. При МРТ исследовании оценка эффективности
препарата проводилась по количеству и объему очагов в Т2-режиме, а также по
количеству очагов, выявляемых при усилении с гадолинием в Т1-режиме. В группе
больных, получавших лечение препаратом Авонекс, количество очагов уменьшилось
на 33 % по сравнению с группой плацебо (р=0.05) (диаграмма №2), объем очагового
поражения мозга также уменьшился (-6.7%) (диаграмма №3), но это различие не
достигло статистической значимости (р=0.36) [19]. Время до наступления подтвержденного
прогрессирования заболевания (первичный критерий) по сравнению с плацебо увеличилось
на 37% (р=0.02) [23].
Исследование эффективности Авонекса в дозе 60 мкг 1 раз в неделю в/м при вторично-прогрессирующем
PC уже закончено, однако к настоящему времени опубликованы только предварительные
результаты [5].
Недавно проведены два прямых открытых рандомизированных сравнительных исследования
оценки эффективности Бетаферона и Авонекса (INCOMIN) и Ребифа и Авонекса (EVIDENCE).
Критериями эффективности в данных исследованиях явились: уменьшение частоты
обострений в год, увеличение пропорции пациентов без обострений заболевания,
уменьшение образования новых активных очагов и общего объема очагового поражения
головного мозга на МРТ.
Исследование INCOMIN - это проспективное,
рандомизированное, многоцентровое исследование, которое не спонсировалось ни
одной фармацевтической компанией, а финансировалось Министерством Здравоохранения
Италии и Итальянским Обществом больных PC. В этом исследовании приняли участие
188 больных с РРС из 15 центров Италии, из которых 92 пациента получали 30 мкг
интерферона бета-1a внутримышечно раз в неделю, и 96 пациентам проводилась терапия
интерфероном бета-1б (Бетаферон) в дозе 250 мкг через день подкожно. После 2-х
лет терапии у 51% больных, получавших лечение интерфероном бета-1б, не наблюдалось
ни одного обострения заболевания по сравнению с 36% больных, получавших интерферон
бета-la (р<0.05) (диаграмма №7). Только у 14% больных, получавших Бетаферон,
наблюдалось прогрессирование заболевания по сравнению с 30% больных, получавших
Авонекс (р<0.05). МРТ обследование и анализ полученных результатов проводились
исследователями в «слепую», т.е. специалисты, оценивавшие МРТ, не имели никакого
представления о том, какой препарат получает больной. Результаты МРТ обследования
показали, что новые Т2-очаги выявлялись у большего количества больных из второй
группы: у 55% больных, получавших интерферон бета-1б, не выявлялось новых очагов
на Т2-изображениях в течение 2-х лет, в то время как, в группе больных, получавших
интерферон бета-1a, подобные результаты наблюдались только у 26% больных (р<0.001).
У 76% больных, получавших Бетаферон, отсутствовали новые очаги, накапливавшие
контраст, по сравнению с 49% пациентов, получавших Авонекс (р=0.001) [7].
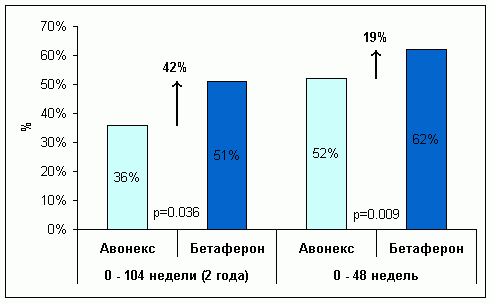
Диаграмма 7. Прямые сравнительные
исследования INCOMIN и EVIDENCE: значимость дозы и частоты введения бета-интерферона.
 |
Другое сравнительное исследование EVIDENCE проводилось в 56 медицинских центрах
Северной Америки и Европы с участием 677 больных с РРС. В этом исследовании
сравнивалась клиническая эффективность двух препаратов - Ребифа в дозе 44 мкг
и Авонекса в дозе 30 мкг. Учитывая, что оба препарата представляют собой интерферон
бета-1а, то различие состояло в том, что пациенты получали разные суммарные
недельные дозы (30 мкг Авонекса или 132 мкг Ребифа), препараты вводились с разной
частотой (Авонекс - 1 раз в неделю и Ребиф - 3 раза в неделю) и разными методами
(внутримышечно или подкожно). Через 24 недели терапии у 75% больных, получавших
Ребиф, не наблюдалось обострений по сравнению с 63% больных, получавших Авонекс,
а через 48 недель 62% и 52% соответственно (р=0.0005 ) (диаграмма №7). Частота
обострений была значительно снижена в группе больных, получавших терапию Ребифом,
по сравнению с группой Авонекса (27%, р=0.02). Клини ческие результаты были
подтверждены данными МРТ у пациентов, получавших Авонекс, было выявлено на 50%
больше активных очагов по сравнению с больными, получавшими Ребиф (р=0.001)
[17].
Сравнительный анализ этих двух исследований
показал, что клинический эффект бета-интерферона зависит от дозы и кратности
введения лекарственного средства. Высокие дозы бета-интерферона, вводимые 3
раза в неделю более эффективны, чем низкие, вводимые 1 раз в неделю. Метод введения
- в/м или п/к не влияют на эффективность препаратов Бетаферон и Ребиф обладают
большей эффективностью для лечения пациентов с PC по сравнению с Авонексом [7,17].
Таким образом, результаты проведенных клинических испытаний всех трех препаратов
бета-интерферона, а также их сравнительный анализ показали:
- Все три препарата бета-интерферона в сравнении с плацебо достоверно снижают
частоту обострений при ремиттирующем течении PC и замедляют прогрессирование
инвалидности, их применение позволяет уменьшить число госпитализаций и проведение
курсов кортикостероидной терапии.
- Эффективность препаратов бета-интерферона зависит от дозы максимальный эффект
обеспечивается максимально высокой переносимой дозой препарата.
- Клинический эффект препарата зависит от частоты введения. Уровень бета-интерферона
в организме должен поддерживаться на определенной границе в течение всей недели.
- Лечение должно быть продолжительным патологический процесс при PC остается
чувствительным к терапии бета-интерфероном длительное время.
- Лечение следует начинать как можно раньше. Раннее начало лечения препаратами
бета-интерферона уменьшает накопление неврологического дефицита и отодвигает
наступление инвалидизации.
Литература
1. Бойко А.Н., Гусев Е.И. Бета-интерфероны при PC. Ж. Неврологии
и Психиатрии, Спец. Выпуск 2002, 65-71
2 Гусев Е.И, Бойко А.Н. Современные подходы к использованию бета-интерферона
в лечении рассеянного склероза. Ж. Неврологии и Психиатрии, 2000; 11: 54-59
3. Н. Allian, S. Schuck. Observations on differences between interferons used
to treat multiple sclerosis. J Clin Res 1998; 1: 381-392
4. Barkhof F., Waesberghe J.H., Filippi M. et al. T1 hypointense lesions in
secondary progressive multiple sclerosis: effect of interferon beta-1 b treatment.
Brain 2001; 124: 1396-1402
5. Cohen J.A., Goodman A.D. Results of IMPACT, a phase 3 trial of interferon
beta-1 a in secondary progressive MS. Neurology 2001; 56 (suppl 3): A148-149
6. European Study Group on Interferon beta-1 b in Secondary Progressive MS.
Placebo-controlled multicenter randomized trial of interferon beta-1b in treatment
of secondary progressive multiple sclerosis. Lancet 1998; 352: 1491-7
7. Durelli L. et al. The INCOMIN Study. Lancet 2002; 359: 1453-1460
8. D.S. Goodin, MD, E.M. Frohman, MD, G.P. Carmany, Jr. et a.l Disease modifying
therapies in multiple sclerosis. Neurology 2002; 58: 169-178
9. IFNB Multiple Sclerosis Study Group. Interferon beta-1b is effective in relapsing-remitting
multiple sclerosis. 1.Clinical results of multicenter, randomised, double-blind,
placebo-controlled trial Neurology. 1993; 43: 655-61
10. The IFNB Multiple Sclerosis Study Group and the University of British Columbia.
MS/MRI Analysis Group Interferon beta-1b in the treatment of multiple sclerosis
final outcome of the randomised controlled trial. Neurology 1995; 45: 1277-85
11. Jacobs L.D., Cookfair D.L., Rudick R.A. et al. Intramuscular interferon
beta-1 a for disease progression in relapsing multiple sclerosis. Ann Neurol
1996; 39: 285-94
12. Li D.H., Paty D.W., UBC MS/MRI Analysis Research Group et al. Magnetic resonance
imaging results of the PRISMS trial randomised, double-blind, placebo-controlled
study of interferon beta-1 a in relapsmg-remitting multiple sclerosis. Ann Neurol
1999; 4: 197-206
13. Li D.H., Zhao G.J., Paty D.W., UBC MS/MRI Analysis Research Group and the
SPECRTIMS Study Group. Randomised controlled trial of interferon-beta-1a in
secondary progressive MS MRI results. Neurology 2001; 56: 1505-1513
14. OWINS Study Group. Evidence of interferon beta-1 a dose response in relapsing
remitting MS. The OWINS study Neurology. 1999; 53: 679-86
15. Paty D.W., Li D.K.B., UBC MS/MRI Study group et al. Interferon beta-1 b
is effective in relapsmg-remitting multiple sclerosis. 2. MRI analysis results
of multicenter, randomised, double-blind, placebo-controlled trial. Neurology
1993; 43: 662-67
16. PRISMS Study Group. Randomised double-blind placebo-controlled study of
interferon beta-1 a in relapsmg-remitting multiple sclerosis. Lancet 1998; 352:
1498-1504
17. H. Panitch, MD, D.S. Goodm, MD, G. Francis, MD et al. Randomized, comparative
study of interferon P -1a treatment regimens in MS. The EVIDENCE Trial. Neurology
2002; 59: 1496-1506
18. PRISMS -4 long-term efficacy of interferon b-1a in relapsing MS. Neurology
2001; 56: 1628 -1636
19. Simon J.H., Jacobs L.D., Campion M. et al. Magnetic resonance studies of
intramuscular interferon beta-1 a for relapsing multiple sclerosis. Ann Neurol
1996; 43: 79-87
20. Simon J.H., Lull J., Jacobs L.D. et al. A longitudinal study of T1 hypointense
lesions in relapsing MS. Neurology 2000; 53: 185-192
21. SPECTRIMS Study Group. Randomised controlled trial of interferon-beta-1a
in secondary progressive MS. Clinical results. Neurology 2001; 56: 1496-1504
22. G.J. Williams, P.L. Witt. Comparative study of the pharmacodynamic and pharmacologic
effects of Betaferon and Avonex. J Int Cyt Res 1998; 18: 967-975
23. Rudick R.A., Godkin D.E., Jacobs L.D. el al. Impact of interferon beta-1
a on neurologic disability in relapsing multiple sclerosis. Neurology 1997;
49: 358-363
24. Sturzebecher S., Mailbauer R., Heuner A. et al. Pharmacodynamic comparison
of single doses of IFNb-1a and IFNb-1b in healthy volunteers. J Int Cyt Res
1999; 19: 1257-1264
25. G.Stok. Oral presentation International symposium. Vienna, 2002
Опубликовано в журнале:
«Нейроиммунология»
2003, №1, стр.45-50
Сайт создан в системе
uCoz